|
|
|
|
|
Контрольная работа
по теме "Молекулярно-кинетическая
теория газов" |
|
|
|
Задачи для самостоятельного решения
по теме "Молекулярно-кинетическая теория газов". |
|
Основные
положения МКТ. |
|
№
6.1




Найти число атомов в алюминиевом предмете массой 135 г.
Решение:
Ответ:
3∙1024. |
|
111 |
|
|
|
№
6.2




Какой объем занимают 100 моль ртути?
Решение:
Ответ:
1,5 л.
|
|
111 |
|
|
|
|
|
№ 6.3.




Зная постоянную Авогадро, найти массу молекулы и атома
водорода.
Решение:
Ответ:3,3∙10-27
кг;
1,7∙10-27
кг.
. |
|
111 |
|
|
|
№
6.4.




Сколько молекул содержится в углекислом газе (СО2)
массой 1 г?
Решение:
Ответ:
1,4∙1022.
|
|
|
|
111 |
|
|
|
№ 6.5.




Какое количество вещества содержится в алюминиевой
отливке массой 5,4 кг?
Решение:
Ответ:200
моль. |
|
111 |
|
|
|
№ 6.6.




Какова масса 500 моль углекислого газа?
Решение:
Ответ:
22 кг. |
|
111 |
|
|
|
№ 6.7.




Из контейнера с твердым литием изъяли 4 моль вещества.
На сколько уменьшилось число молекул лития в контейнере?
Решение:
Ответ:
24∙1023. |
|
111 |
|
|
|
№ 6.8.




Считая, что диаметр молекул водорода составляет около
2,3∙10-10 м,
подсчитать, какой длины получилась бы нить, если бы все
молекулы, содержащиеся в 1 мг этого газа, были
расположены в один ряд вплотную друг к другу.
Сопоставить длину этой нити со средним расстоянием от
Земли до Луны.
Решение:
Ответ:6,9∙1010; длина нити в 180 раз больше. |
|
111 |
|
|
|
№ 6.9.




Находившаяся в стакане вода массой 200 г полностью
испарилась за 20 суток. Сколько в среднем молекул воды
вылетало с ее поверхности за 1 с?
Решение:
Ответ:
3,9∙1018.. |
|
111 |
|
|
|
№ 6.10.




В озеро, имеющее среднюю глубину 10 м и площадь
поверхности 20 км2, бросили кристаллик
поваренной соли массой 0,01 г. Сколько молекул этой соли
оказалось бы в наперстке воды объемом 2 см3,
зачерпнутой из озера, если полагать, что соль,
растворившись, равномерно распределилась во всем объеме
воды озера?
Решение:
Ответ:
около 106. |
|
111 |
|
|
|
№ 6.11.




На изделие, поверхность которого 20 см2,
нанесен слой серебра толщиной 1 мкм. Сколько атомов
серебра содержится в покрытии?
Решение:
Ответ: В покрытии содержится примерно 1,2∙1020. |
|
111 |
|
|
|
№ 6.12.




Какова температура кипения воды при нормальных условиях
по абсолютной шкале температур?
Решение:
Ответ:373 К. |
|
111 |
|
|
|
№ 6.13.




В таблице указана плотность газов при нормальном
атмосферном давлении.Молекулы, какого газа при этом имеют наибольшую
среднеквадратичную скорость?

Решение:
Ответ:
Наибольшую скорость имеют молекулы
водорода.. |
|
111 |
|
|
|
№ 6.14.




В таблице указана плотность газов при нормальном
атмосферном давлении.
Молекулы, какого газа при этом имеют наименьшую
среднеквадратичную скорость?

Решение:
Ответ:
Наименьшую скорость имеют молекулы ксенона. |
|
111 |
|
|
|
№ 6.15.




Найти концентрацию молекул кислорода, если при давлении
0,2 МПа средняя квадратичная скорость его молекул равна
700 м/с.
Решение:
Ответ:2,3∙1025 м-3.. |
|
111 |
|
|
|
№ 6.16.




Каково давление газа, если средняя квадратичная
скорость его молекул 500 м/с, а его плотность 1,35 кг/м3?
Решение:
Ответ:
Давление газа составляет примерно 0,11 МПа.. |
|
111 |
|
|
|
№ 6.17.




При какой температуре средняя кинетическая энергия
поступательного движения молекул газа равна 6,21∙10-21Дж?Решение:
Ответ:При температуре 27˚С средняя кинетическая энергия
движения молекул газа равна 6,21∙10-21Дж. |
|
111 |
|
|
|
№ 6.18.




При температуре 263 K и давлении 1,5∙105 Па
плотность газа равна 2 кг/м3. Какова молярная
масса этого газа? Ответ приведите в кг/моль.
Решение:
Ответ:
Молярная масса газа равна 0,029 кг/моль.. |
|
111 |
|
|
|
№ 6.19.




Какова средняя квадратичная скорость движения молекул
газа, если, имея массу 6 кг, он занимает объем 5 м3
при давлении 200 кПа?
Решение:
Ответ:710 м/с.. |
|
111 |
|
|
|
№ 6.20.




При неизменном давлении одноатомного идеального газа
среднеквадратичная скорость движения его атомов
увеличилась в 4 раза. Как при этом изменилась плотность
газа?
Решение:
Ответ:
уменьшилась в 16 раз. |
|
111 |
|
|
|
№ 6.21.




Средняя кинетическая энергия поступательного движения
молекул одноатомного идеального газа, при температуре 27°С,
равна Е1. Чему будет равна средняя
кинетическая энергия молекул этого газа, если
температура повысится до 327°С?
Решение:
Ответ:2Е1 |
|
111 |
|
|
|
№ 6.22.




Найти среднюю кинетическую энергию молекулы одноатомного
газа при давлении 20 кПа. Концентрация молекул этого
газа при указанном давлении составляет 3∙1025м-3.
Решение:
Ответ:10-21
Дж.. |
|
111 |
|
|
|
№ 6.23.




При какой температуре средняя кинетическая энергия
молекул одноатомного газа будет в 2 раза больше, чем при
температуре -73 °С?
Решение:
Ответ:127˚С.. |
|
111 |
|
|
|
№ 6.24.




Найти среднюю квадратичную скорость молекулы водорода
при температуре 27 °С.
Решение:
Ответ:1,9 км/с. |
|
111 |
|
|
|
№ 6.25.




Во сколько раз средняя квадратичная скорость молекул
кислорода меньше средней квадратичной скорости молекул
водорода, если температуры этих газов одинаковы?
Решение:
Ответ:
в 4 раза. |
|
111 |
|
|
|
№ 6.26.




При какой температуре средняя квадратичная скорость
молекул азота равна 830 м/с?
Решение:
Ответ:
774 К |
|
111 |
|
|
|
№ 6.27.




Во сколько раз средняя квадратичная скорость молекул
водяного пара в летний день при температуре 30°С больше,
чем в зимний день при температуре - 30°С?
Решение:
Ответ:
в 1,12 раза. |
|
111 |
|
|
|
№ 6.28.




Решение:
Ответ:127˚С.. |
|
111 |
|
|
|
№ 6.29.




Решение:
Ответ:127˚С.. |
|
111 |
|
|
|
№ 6.30.




Решение:
Ответ:127˚С.. |
|
111 |
|
|
|
|
|
Газовые
законы |
|
№ 6.31.




В баллоне находятся 20 кг азота при температуре 300 К и
давлении 105
Па. Каков объем баллона? Ответ округлите до
целых.
Решение:
Ответ:
Объем газа составляет примерно 18 м3.
|
|
111 |
|
|
|
№ 6.32.




Идеальный газ в цилиндре
переводится из состояния А в состоянии В
так, что его
масса при этом не изменяется. Параметры, определяющие
состояния газа, приведены в таблице.
Какое число
следует внести в свободную клетку таблицы?

Решение:
Ответ:
В свободную клетку таблицы следует вписать число 300.
|
|
111 |
|
|
|
№ 6.33.




Воздух объемом 1,45 м3,
находящийся при температуре 20°С и давлении 100 кПа,
перевели в жидкое состояние. Какой объем займет жидкий
воздух, если его плотность 861 кг/м3?
Решение:
Ответ:
Жидкий воздух займет объем 2 л.
|
|
111 |
|
|
|
№ 6.34.




В
сосуде находится некоторое количество идеального газа.
Как изменится температура
газа, если он перейдет из состояния 1 в состояние 2 (см.
рисунок)?
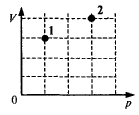
Решение:
Ответ:
Температура в состоянии 2 в 4 раза больше температуры
в состоянии 1.
|
|
111 |
|
|
|
№ 6.35.




Какое количество вещества содержится в газе, если при
давлении 200 кПа и температуре 240 К его объем равен 40
л?
Решение:
Ответ:
4 моль.
|
|
111 |
|
|
|
№ 6.36.




Каково давление сжатого воздуха, находящегося в баллоне
вместимостью 20 л при температуре 12 °С, если масса
этого воздуха 2 кг?
Решение:
Ответ:
8,2 МПа
|
|
111 |
|
|
|
№ 6.37.




В комнате площадью S = 20 м2
и высотой h = 2,5 м температура воздуха повысилась с Т1
= 288 К до Т2
= 298 К. Давление постоянно и равно р = 100 кПа. На
какую величину ∆m уменьшилась масса воздуха в комнате?
Решение:
Ответ:
2 кг.
|
|
111 |
|
|
|
№ 6.38.




Найти массу природного горючего газа объемом 64 м3,
считая, что объем указан при нормальных условиях.
Молярную массу природного горючего газа считать равной
молярной массе метана (СН4).
Решение:
Ответ:
45,7 кг.
|
|
111 |
|
|
|
№ 6.39.




В баллоне емкостью 20 л находится кислород при температуре 16ºС под
давлением 107 Па. Какой объем займет этот газ
при нормальных условиях? Ответ выразите в кубических
метрах и округлите с точностью до сотых.
Решение:
Ответ:
1,89 м3.
|
|
111 |
|
|
|
№ 6.40.




В баллоне находится газ при температуре 15 °С. Во
сколько раз уменьшится давление газа, если 40% его
выйдет из баллона, а температура при этом понизится на 8
°С?
Решение:
Ответ:
в 1,7 раза.
|
|
111 |
|
|
|
№ 6.41.




На поверхности Венеры температура и атмосферное давление
соответственно равны 750 К и 9120 кПа. Найти плотность
атмосферы у поверхности планеты, считая, что она состоит
из углекислого газа.
Решение:
Ответ:
64,4 кг/м3.
|
|
111 |
|
|
|
№ 6.42.




Какова при нормальных условиях плотность смеси газов,
состоящей из азота (N2)
массой 56 г и углекислого газа (СО2)
массой 44 г?
Решение:
Ответ:
1,49 кг/м3.
|
|
111 |
|
|
|
№ 6.43.




В баллоне вместимостью 25 л находится смесь газов,
состоящая из аргона (Аг) массой 20 г и гелия (Не) массой
2 г при температуре 301 К. Найти давление смеси газов на
стенки сосуда.
Решение:
Ответ:
100 кПа..
|
|
111 |
|
|
|
№ 6.44.




Определить плотность смеси, состоящей из 4 г водорода и
32 г кислорода, при температуре 7˚С и давлении 93 кПа.
Решение:
Ответ:
Плотность смеси газов равна 0,48 кг/м3..
|
|
111 |
|
|
|
№ 6.45.




Метан подают по газопроводу при давлении 405,2 кПа и
температуре 300 К, причем через поперечное сечение трубы
площадью 8 см2
за 20 мин проходит 8,4 кг газа. Определить скорость
протекания газа по трубе.
Решение:
Ответ:
3,36 м/с. |
|
111 |
|
|
|
Изотермический
процесс. |
|
№ 6.46.




При сжатии газа его объем уменьшился с 8 до 5 л, а
давление повысилось на 60 кПа. Найти первоначальное
давление.
Решение:
Ответ:
100 кПа.
|
|
111 |
|
|
|
№ 6.47.




При увеличении давления в 1,5 раза объем газа уменьшился
на 30 мл. Найти первоначальный объем.
Решение:
Ответ:90 мл. |
|
111 |
|
|
|
№ 6.48.




Пузырек воздуха всплывает со дна водоема. На глубине 6 м
он имел объем 10 мм3.
Найти объем пузырька у поверхности воды.
Решение:
Ответ:16 мм2. |
|
111 |
|
|
|
№ 6.49.




Площадь поршня (см. рис.) равна 24 см2,
объем воздуха в цилиндре 240 см3,
а давление равно атмосферному 100 кПа. Какую силу надо
приложить, чтобы удерживать поршень после его смещения
на 2 см:
а) влево;
б) вправо?
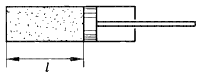
Решение:
Ответ:60 Н; 40 Н. |
|
111 |
|
|
|
№ 6.50.




Решение:
Ответ: |
|
111 |
|
|
|
Изобарный процесс. |
|
№ 6.51.




Какой объем займет газ при температуре 77 °С, если при
температуре 27 °С его объем был 6 л?
Решение:
Ответ:
7 л.
|
|
111 |
|
|
|
№ 6.52.




При увеличении абсолютной температуры в 1,4 раза объем
газа увеличился на 40 см3.
Найти первоначальный объем газа.
Решение:
Ответ:
100 см3..
|
|
111 |
|
|
|
№ 6.53.




Температура воздуха в цилиндре (см. рис.) 7 °С. На
сколько переместится поршень при нагревании воздуха на
20 К, если
l
= 14 см?

Решение:
Ответ:
на 1 см.
|
|
111 |
|
|
|
№ 6.54.




Какова была начальная температура воздуха, если при
нагревании его на 3 К объем увеличился на 1% от
первоначального?
Решение:
Ответ:
27˚С.
|
|
111 |
|
|
|
№ 6.55.




Решение:
Ответ:
|
|
111 |
|
|
|
Изохорный процесс. |
|
№ 6.56.




При температуре 27 °С давление газа в закрытом сосуде
было 75 кПа. Каким будет давление при температуре -13
°С?
Решение:
Ответ:
65 кПа.
|
|
111 |
|
|
|
№ 6.57.




В нерабочем состоянии при температуре 7 °С давление газа
в колбе газополной электрической лампы накаливания равно
80 кПа. Найти температуру газа в горящей лампе, если
давление в рабочем режиме возрастает до 100 кПа.
Решение:
Ответ:
77˚С..
|
|
111 |
|
|
|
№ 6.58.




Давление воздуха в автомобильной камере при температуре
-13 °С было 160 кПа (избыточное над атмосферным). Каким
стало давление, если в результате длительного движения
автомобиля воздух в камере нагрелся до 37 °С?
Решение:
Ответ:
190 кПа..
|
|
111 |
|
|
|
№ 6.59.




При какой температуре находился газ в закрытом сосуде,
если при нагревании его на 140 К давление возросло в 1,5
раза?
Решение:
Ответ:
7˚С..
|
|
111 |
|
|
|
№ 6.60.




Бутылка, наполненная газом, плотно закрыта пробкой
площадью сечения 2,5 см2.
До какой температуры надо нагреть газ, чтобы пробка
вылетела из бутылки, если сила трения, удерживающая
пробку, 12 Н? Первоначальное давление воздуха в бутылке
и наружное давление одинаковы и равны 100 кПа, а
начальная температура равна -3 °С.
Решение:
Ответ:
127˚С.
|
|
111 |
|
|
|
№ 6.61.




Решение:
Ответ:
40 м.
|
|
111 |
|
|
|
№ 6.62.




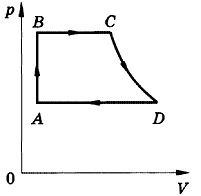
|
На рисунке представлен замкнутый цикл. Участок CD
соответствует изотерме. Вычертить эту диаграмму в
координатах рТ и
VТ.
Решение:
Ответ:
.
|
 |
|
|
111 |
|
|
|
№ 6.63.




В сосуде, закрытом поршнем находится идеальный газ. На
рисунке показан график зависимости объема газа от
температуры. В каком состоянии давление газа наибольшее?
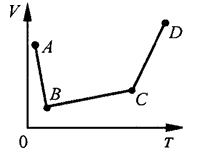
Решение:
Ответ:
В состоянии С.
|
|
111 |
|
|
|
Влажность воздуха |
|
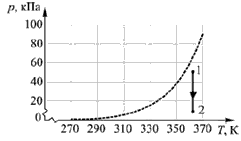
№ 6.64.




На рисунке изображены: пунктирной линией — график
зависимости давления Р насыщенных паров воды от
температуры Т, и сплошной линией — процесс 1-2
изменения парциального давления паров воды.
Как
изменяется по мере такого изменения парциального
давления паров воды абсолютная влажность воздуха?
Решение:
Ответ:
В процессе 1 – 2 абсолютная влажность воздуха
уменьшается.
|
|
111 |
|
|
|
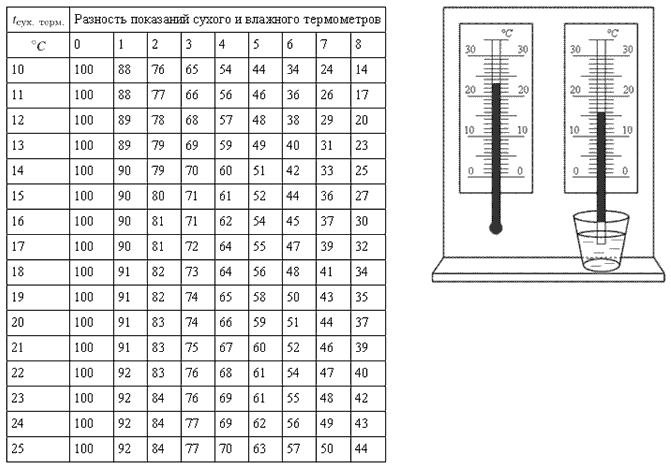
№ 6.65.




На фотографии представлены два термометра, используемые
для определения относительной влажности в помещении с
помощью психрометрической таблицы, в которой влажность
указана в процентах. Чему равна относительная влажность
воздуха в помещении, где проводилась съемка?
Решение:
Ответ:
48%
|
|
111 |
|
|
|
№ 6.66.




Давление пара в
помещении при температуре 5°С
равно 756 Па. Давление насыщенного пара при этой
температуре равно 880 Па. Какова относительная влажность
воздуха в помещении?
Решение:
Ответ:
86%.
|
|
111 |
|
|
|
№ 6.67.




Относительная
влажность воздуха в помещении при температуре 20°С
составляет 42%. Парциальное давление при этой
температуре составило 980 Па. Чему равно давление
насыщенного пара при заданной температуре?
Решение:
Ответ:
2333 Па.
|
|
111 |
|
|
|
№ 6.68.




Относительная
влажность воздуха в цилиндре под поршнем равна 60%.
Воздух изотермически сжали, уменьшив объем в два раза.
Чему стала равна относительная влажность воздуха в
сосуде под поршнем.
Решение:
Ответ:
100%.
|
|
111 |
|
|
|
№ 6.69.




Определите плотность водяного пара при температуре 100°С
и относительной влажности 30%? Ответ запишите с
точностью до сотых.
Решение:
Ответ:
0,17 кг/м3. |
|
111 |
|
|
|
№ 6.70.




В
комнате размерами 4×5×3 м, в которой воздух имеет
температуру 10 °C и относительную влажность 30 %,
включили увлажнитель воздуха производительностью 0,2
л/ч. Чему станет равна относительная влажность воздуха в
комнате через 1,5 ч? Давление насыщенного водяного пара
при температуре 10 °C равно 1,23 кПа. Комнату считать
герметичным сосудом.
Решение:
Ответ: 83%. |
|
111 |
|
|
|
Задачи повышенной сложности. |
|
№ 6.75.




Воздушный шар, оболочка которого имеет массу М =
145 кг и объем V = 230 м3,
наполняется горячим воздухом при нормальном атмосферном
давлении и температуре окружающего воздуха 0˚С. Какую
минимальную температуру должен иметь воздух внутри
оболочки, чтобы шар начал подниматься? Оболочка шара
нерастяжима и имеет в нижней части небольшое отверстие.
Решение:
Ответ:
Минимальная температура, до которой нужно нагреть воздух
в шаре, чтобы он начал подниматься, равна 265˚С.
|
|
111 |
|
|
|
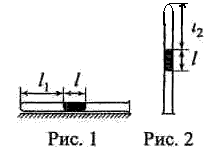
№ 6.76.




В трубке, расположенной
горизонтально, находится столбик воздуха длиной 30,7 см,
запертый столбиком ртути длиной 21,6 см (рисунок 1).
Какой будет длина воздушного столбика над ртутью, если
трубку поставить вертикально отверстием вниз (рисунок
2)? Атмосферное давление 747 мм рт. ст.; 1 мм рт. ст.=
133 Па. Температуру воздуха в пробирке считать
постоянной.
Решение:
Ответ:
43,2
см..
|
|
111 |
|
|
|
№ 6.77.




Пузырек воздуха всплывает со дна озера к поверхности,
при этом его объем увеличивается в 3 раза. Какова
глубина озера? Температуру воды считать одинаковой по
всей глубине озера.
Решение:
Ответ:
Глубина озера составляет 20 м. |
|
111 |
|
|
|
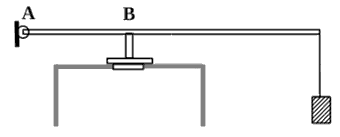
№ 6.78.




В цилиндр закачивается воздух со скоростью 0,002 кг/с. В
верхнем торце цилиндра есть отверстие площадью 5∙10-4
м2, закрытое предохранительным клапаном.
Клапан удерживается в закрытом состоянии невесомым
стержнем длиной 0,5 м, который может свободно
поворачиваться вокруг оси в точке А (см. рисунок).
Расстояние АВ равно 0,1 м. К свободному концу стержня
подвешен груз массой 2 кг. Клапан открывается через 580
с работы насоса, если в начальный момент времени
давление воздуха в цилиндре было равно атмосферному.
Температура воздуха в цилиндре и снаружи не меняется и
равна 300 К. Определите объём цилиндра.
Решение:
Ответ:
Объем цилиндра равен 0,5 м3..
|
|
111 |
|
|
|
№ 6.79.




Решение:
Ответ:
333 Дж.
|
|
111 |
|
|
|
№ 6.80.




Решение:
Ответ:
КПД системы блоков равен 91%.
|
|
111 |
|
|
|
№ 6.77.




|
|
111 |
|
|
|
№ 6.78.




|
|
111 |
|
|
|
№ 6.50.




Решение:
Ответ: |
|
111 |
|
|
|
|
|
|
|
|
|
№ 6.79.




|
|
111 |
|
|
|
№ 6.80.




|
|
111 |
|
|
|
Задачи
повышенной сложности. |
|
№ 6.81.




|
|
Решение:
|
|
Ответ: . |
|
111 |
|
|
|
№ 6.82.




Решение:
Ответ:
.
|
|
111 |
|
|
|
№ 6.83.




|
|
111 |
|
|
|
№ 6.84.




|
|
111 |
|
|
|
№ 6.85.




|
|
111 |
|
|
|
№ 6.86.




|
|
111 |
|
|
|
№ 6.87.




|
|
111 |
|
|
|
|
|
|
|
|
|
Содержание |
| |
|
|
